한미약품 '롤론티스' 10년만에 FDA 시판 승인오는 4분기, 미국 시장 공략···점유율 2% 전망증권가 "신약 판매는 새로운 이익 성장 동력"
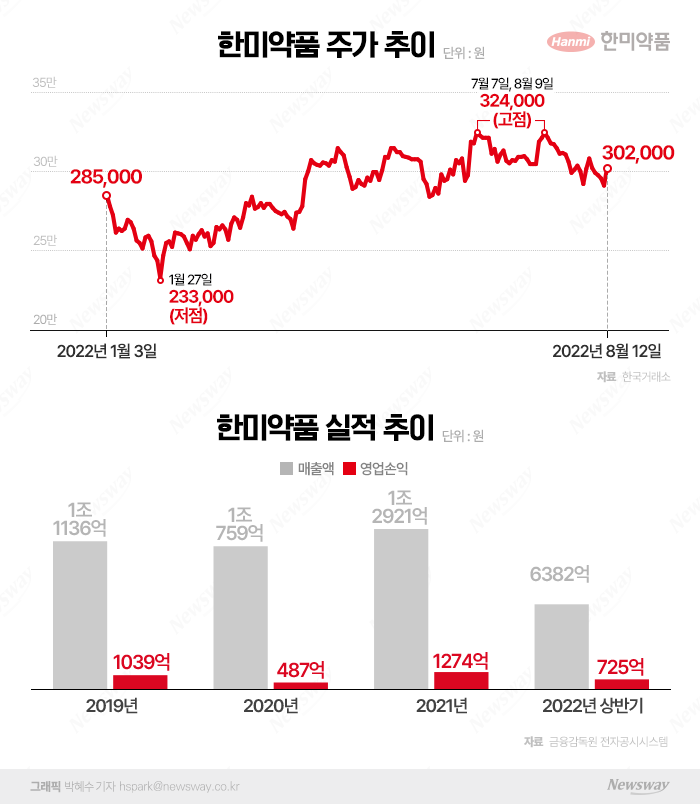
13일 한국거래소에 따르면 한미약품은 전 거래일 대비 3000원(0.99%) 오른 30만5000원에 거래를 마쳤다. 이날 한미약품의 장중 고가는 32만6500원으로 오후 들어 상승세가 소폭 감소했으나 여전히 전 거래일 대비 증가세를 보였다.
이번 미국 FDA의 허가를 받은 신약은 지속형 호중구(백혈구의 한 유형)감소증 치료제인 '롤론티스'다. 한미약품은 지난 2012년 스펙트럼(Spectrum pharmaceuticals)에 기술 이전을 한 이후 10년만에 FDA로부터 승인을 획득했다.
롤론티스는 국내 한미약품 평택 공장에서 생산해 미국으로 수출하는 첫 국내 신약이다. 한미약품 신약이 FDA의 허가를 받은 것은 최초이며, 국내 업계에서는 여섯번째다. 롤론티스는 오는 4분기부터 '롤베돈(Rolvedon)' 이라는 제품명으로 미국에서 판매될 예정이다.
시장에서는 향후 한미약품의 주가에 촉각을 곤두세우고 있다. 미국에서의 호중구감소증 시장 규모는 약 4조원대로, 한미약품은 이번 시판 허가에 따라 본격적인 시장 공략에 나설 것으로 알려졌다.
한미약품의 내년 롤론티스 미국 매출액은 약 6000만달러로, 시장 점유율 2% 수준을 차지할 것으로 추정된다. 여기에 스펙트럼사를 통해 한미약품으로 유입되는 로열티는 생산 마진 제외 기준 약 40억원 이상으로, 투자업계에서는 매출 확대에 따른 영업 레버리지 개선 및 수익성 확대가 가능할 것이라고 판단하고 있다.
이번 롤론티스의 FDA 승인 이후 오는 11월 비소세포폐암 치료제인 포지오티닙(Poziotinib)의 PDUFA(Prescription Drug User Fee Act) 승인 역시 기대를 받고 있다. 업계에서는 이번 유럽종양학회(ESMO) 결과를 바탕으로 승인이 될 확률이 높은 것으로 알려졌다. 국내 자체 개발 신약이 글로벌 허가 승인까지 이어질 수 있어, 주가 상승 모멘텀으로 작용할 것이라는 전망이다.
임윤진 대신증권 연구원은 "자체개발 지속형 플랫폼 '랩스커버리' 신약의 첫 FDA 시판허가로 동사의 R&D 기술력 입증했다"며 "평택 바이오공장의 성공적인 FDA 실사 완료는 후속 랩스커버리 파이프라인 개발 시 긍정적 작용할 것"이라고 예상했다. 이어 "2019년 이후 3년만에 국내 개발 신약의 FDA 시판허가 획득에 따라 신약개발 기업에 대한 투자심리 회복도 기대된다"고 밝혔다.
권해순 유진투자증권 연구원은 "롤론티스와 포지오티닙의 미국 판매가 향후 한미약품의 내수 부분 성장 둔화 가능성을 상쇄시킬 수 있는 새로운 이익 성장 동력이라고 판단한다"며 "올해 4분기 혹은 내년 출시를 가정할 경우, 출시 5년차인 2027년 제품 합산 매출액은 약 4500억원, 한미약품으로 반영되는 이익은 영업이익 기준 약 600억원에 달할 것"이라고 추정했다.

뉴스웨이 안윤해 기자
runhai@newsway.co.kr
<저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지>






















댓글